原子结构示意图: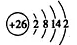 ;核外电子排布式:1s2s22p63s23p63d64s2;
;核外电子排布式:1s2s22p63s23p63d64s2;
Fe2+结构示意图: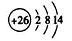 ;核外电子排布式:1s2s22p63s23p63d6;
;核外电子排布式:1s2s22p63s23p63d6;
Fe3+结构示意图: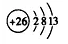 ;核外电子排布式:1s2s22p63s23p63d5;
;核外电子排布式:1s2s22p63s23p63d5;
第三层是14的原因是:根据能量最低原理,排布电子时,要先排布4s轨道,然后嫌腔再排布3d轨道。
原子结构示意图是表示原子核电荷数和电子层排布的图示形式。小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数。
扩展资料:
(1)原子结芹歼衫构示意图的认识
①不是所有原子都是由质子、中子、电子构成的:氢原子中改厅没有中子。
②原子不显电性:由于核内的1个质子带一个单位正电荷,原子核带正电,带的正电荷数与核外的电子数相等,所以原子不显电性,因此分子也不显电性。
③核电荷数:原子核带的正电荷数。
(2)在原子中 核电荷数=质子数=核外电子数
(3)原子的质量主要集中在 原子核上
(4)相对原子质量≈质子数+中子数
(5)相对原子质量:以一种碳原子的质量的1/12为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量。
参考资料:百度百科-原子结构示意图



