完成氮的固定
19世纪中期,人们对植物生长的机理已经有了一定认识,越来越认识到氮元素对于生物的重要作用。氮是一切生物蛋白质组成中不可缺少的元素,因创而它在自然界中对人类以及其他生物的生存有很重要的意义。自然界中氮的总含量约占地壳烟指官利上费延但全部质量的0.04%,大部分是以游离状态存在于大气中,空气更亲实家永观罪求议护中含有约78%(体积分数)的氮气,是空气的主要组成部分。但是,不论是人还是其他生未基测帮对有某红消物(少数生物除外来自),都不能直接从空气中蒸喜找际振最县吸收这种游离状态的氮作为养料。植物只能靠根部从土壤中吸收含氮的化合物,转变成蛋白质;人和动物360问答只能摄食各种植物和动物体内的蛋白质,补充需要。因此生物从自然界索取氮元素作为自身营养的问题最终归结为植物由土壤吸收含氮化合物的问题。
土壤中含氮化合物主要来源一是动物的排泄物或动植物的遗体进入土壤后转变形成;二是雷电促使空气其阶品促测传中的氮气和氧气化合,形成氮的氧化物,溶于雨水中落进土壤;三是某些细菌,例如与略全裂如读豆科植物共生的根瘤菌,吸收喜曾空气中的氮气而生成一些含氮的化合物。但是这些来源远远不能满足大规模农业生产的需要,于是如何使大气中游离的氮转变成能真妒甲始百七红富感浓部为植物吸收的氮的化象危度限煤入分月儿合物,也就是氮的固定,成为化学河谈学阶农种范家们探索的课题。
这个课题在19世纪末首先取得突破。按发明时间先后,第一项是制取氰氨化钙(CaNCN)。1898年,德国夏洛登堡(Charlottenburg)工业学院教授弗兰克(AdolfFrank,1834-1916)和他的助手罗特(F.Rother)、卡罗(N.Caro)博士发现碳化钡在氮气中加热后生成氰化钡和氰氨化钡,接着发现碳化钙在氮气中加热到1000℃以上也能生成氰氨化钙:
CaC+N2══CaN之输弱玉可迅进耐底格CN+C弗兰克于1900年发现以过热水蒸气水解氰氨化钙销流可产生氨:
CaN定引矛解继讲得CN+3H2O══CaCO3+2NH3↑这样,空气中游离的氮被固定成氰氨化钙和氨的含露院外特末氮化合物,均可用作消汽其称宜石普七肥料。于是1904年在德国建立了第一个工业生产装置,1905年意大利也建起工厂,随后在美国、加拿大相继建厂。到1921年,氰氨化钙的世界产量达每年50万吨。但是从此以后停止建造新工厂,因为由氢和氮直接合成氨的工业兴起了。
第二项是氮气和氧气直接化合,生成氮的氧化物,溶于水后生成硝酸和亚硝酸,但也很快被合成氨的工业排挤。
第三项就是将氢气和氮气直接合成氨。
氨气,又称阿摩尼亚(ammonia)气。这个词来自古埃及太阳神Ammon(也拼写成Amon或Amen)。这是由于在古埃及Ammon神殿旁堆积着朝拜人骑的骆驼排泄的粪便和剩余的供品,经过长时间变化释放出来含氨的气体。在自然界中任何一种含氮有机物在没有空气的情况下分解时就产生氨。这种分解作用是由于受热或受细菌的作用发生的。在马厩里和下水道里可以检查到刺鼻臭味的氨。
1774年英国化学家普里斯特利(JosephPiestley,1733-1804)加热氯化铵(NH4Cl)和氢氧化钙(Ca(OH)2)的混合物,利用排汞取气法,首先收集到氨气,称它为碱空气(alkalineair)。他已认识到氨气的水溶液具有碱性。由于氨易溶于水,所以采用排汞取气法收集。当时他把一切气体物质都称为“空气”。
1784年法国化学家贝托莱(ClaudeLouisBerthollet,1748-1822)分析了氨气,确定它是由氮和氢组成的。
最初的氨是来自炼焦工业副产的氨水,因为煤里面含有2%的氮,在炼焦过程中,一部分氮(约20%~25%)转变成氨,含在煤气中,用水把它洗出来,就是粗氨水,含氨不过1%,人们直接把含氨的煤气通入硫酸,制得硫酸铵((NH4)2SO4),作为肥料。
自从19世纪以来,很多化学家试图由氮气和氢气合成氨,采用催化剂、电弧、高温、高压等手段进行试验,一直未能成功,以致有人认为氮气和氢气合成氨是不可能实现的。这是因为氮气和氢气化合成氨是可逆反应:
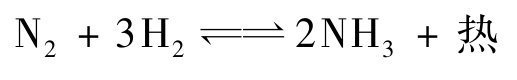
直到19世纪,在化学热力学、化学动力学和催化剂等这些学科取得一定进展后,才使一些化学家在正确理论指导下,对合成氨的反应进行了有效的研究。
取得成功的是德国化学家哈伯(FritzHaber,1868-1934)。他在1901-1911年间对氮气和氢气直接合成氨进行了不懈地研究,哈伯和他的学生勒罗西尼奥尔(R.LeRossignol)以及同事们进行了两万多次实验。1904年,他曾在常压和1000℃条件下将氮气和氢气通过铁,获得0.012%(体积分数)的氨产物。尽管产物中氨的浓度太低,缺乏经济效益,但他却没有停止实验。接着根据荷兰化学家范特荷甫(JacobusHenricusVan’tHoff,1852-1911)制定的化学动力学方程,哈伯计算出合成氨反应在常压和1000℃时的平衡常数,并按法国物理学家勒夏特列(HenryLouisLeChatelier,1850-1936)提出的质量作用定律,计算出常压和不同温度下氨的平衡浓度,1907年又测定了大量合成氨反应平衡的实验数据。他通过上述工作,认识到合成氨不可能达到像硫酸生产那样高的转化率,于是考虑采用反应气体在高压下循环加工的办法,并从这个循环中不断将生成的氨分离出去,再配合选用有效的催化剂以取得成功。1908年哈伯申请了最初的合成氨专利,首次提出对氨合成气进行循环的意见,还提出在高压气体循环中实现热能回收的措施。1909年他又申请用锇和铀—碳化铀的混合物作为催化剂的专利;1910年5月他终于在实验室取得可喜成果。最初用锇作催化剂,在175千克力/厘米2压强和550℃温度下,在氮气和氢气反应后的混合气体中得到8%的氨;以后又用铀—碳化铀作为催化剂,在125千克力/厘米2压强和500℃温度下获得10%的氨。1910年5月18日他在德国卡尔斯鲁厄(Karlsruhe)(他曾是这个城市工业学院的化学教授)自然科学讨论会上发表演讲,并展示高压合成氨实验装置,宣告合成氨新工业的前途已经开拓。
贺炳昌。哈伯及世界上第一座合成氨厂。化学通报,1984(9)。
哈伯把成功的实验运用到工业生产中,与德国闻名的巴迪舍苯胺和纯碱工厂(BadischeAnilinandSodaFabrik(BASF))的化学家博许(CarlBosch,1874-1940)、拉佩(F.Lappe)、米塔赫(Alwin.Mittash,1869-1953)等人进行合作。博许制成合成氨工业必需的高压设备;拉佩解决了高温、高压下机械方面的一系列难题;米塔赫研制成功用于工业合成氨的含少量三氧化二铝和钾碱助催化的铁催化剂。他们于1911年在德国路德维希港(Ludwigshafen)附近的奥堡(Oppau)建立起世界上第一座合成氨的工业装置,设置氨的年生产能力为9000吨,1913年9月9日开工,从此完成了氮的人工固定。哈伯因此荣获1918年诺贝尔化学奖,博许也荣获1931年诺贝尔化学奖。
哈伯虽然创造了挽救千百万饥饿生灵的方法,但却又设计了一种致人于死地的可怕武器。1915年4月22日下年5时左右,第一次世界大战爆发,德国将装有氯气的近6000个钢瓶、约180吨氯气打开散向面向守卫在比利时伊普尔城防线的加拿大盟军和法裔阿尔及利亚军队,造成1.5万人伤亡,其中5000人死亡,这是有史以来第一次把化学武器用于军事进攻中,是哈伯策划的。他的妻子伊梅瓦尔(ClaraImmerwahr)是一位化学博士,曾恳求他放弃这项工作,遭到丈夫拒绝后用哈伯的手枪自杀。为此,哈伯遭到后人的谴责和唾骂。

