阿伏加德罗定律:同温同压下,相同体积的任何气体含有相同的分子数,称为阿伏加德罗定律。气体的体积是指所含分子占据的空间,通常条件下,气体分子间的平均距离约为分子直径的10倍,因此,当气体所含分子数确定后,气体的体积主要决定于分子间的平均距离而不是分子本身的大小。
在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子,所以又叫四同定律,也叫五同定律或克拉贝隆方程(五同指同温、同压、同体积、同分子个数、同物质的量)。
公式:PV=nRT,P表示压强、V表示气体体积、n表示物质的量、T表示绝对温度、R表示气体常数。所有气体R值均相衡搏罩同。如果压强、温度和体积都采用银瞎国际单位(SI),R=8.31帕·米3/摩尔·开。
推论:
(2)同温同体积时, 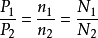 (压强比等于物质的量之比等于分子数之比)
(压强比等于物质的量之比等于分子数之比)
(咐闹4)同温同压时,M1/M2=P1/P2





